심혈관계 시뮬레이터를 이용한 중심-상완 혈압 파형 재현
© The Korean Society for Noise and Vibration Engineering
Abstract
With the increase in the importance of cardiovascular health, the correlation with blood pressure, the most important indicator, is being actively studied. Therefore, blood pressure waveform data are essential. However, the clinical measurement of blood pressure has limitations with respect to the amount and distribution of data because blood pressure is measured invasively over the artery. The cardiovascular simulator in this study mimics the structure and properties of human arteries. It reproduces the generation of blood pressure waveforms owing to the overlap of forward and reflected waves. The reproduced central–brachial–radial blood pressure waveforms are similar to those of a human in magnitude, shape, and characteristics. When the blood pressure waveform propagates from the central to the radial artery, the waveform changes owing to systolic amplification and a reduced overlap area is reproduced. The developed cardiovascular simulator can supplement missing links in clinical data. This can be expanded to medical devices and health sensor testing platforms as a core technology for future cardiovascular health-related research.
Keywords:
Cardiovascular, Simulator, Blood Pressure, Waveform, Central Aorta, Radial Artery키워드:
심혈관, 시뮬레이터, 혈압, 파형, 중심 대동맥, 요골 동맥1. 서 론
세계 10대 사망 원인 중 1, 2위는 심혈관계 관련 질환이며, 그에 따른 심혈관계 건강 관리의 중요성이 대두되고 있다(1). 때문에 ECG, PPG 등 생체신호를 바탕으로 심혈관계 건강 상태를 추정하는 헬스 센서, AI 관련 연구가 활발히 진행되고 있다(2). 심혈관계 건강 지표 중 가장 중요하게 다뤄지는 것은 혈압으로, 심박수, 박출량 등 심혈관계 건강 상태에 따라 최고, 최저 혈압뿐만 아니라 그 파형이 결정된다고 알려져 있다(3).
이를 바탕으로 혈압 파형과 심혈관계 건강상태 사이의 상관관계에 대한 임상 기반 연구가 활발히 진행되었다(4). 그러나 혈압 파형은 동맥에 침습적으로 카테터를 삽입하여 측정되어야 하며, 따라서 임상 데이터의 그 양과 질이 절대적으로 부족하다. 이러한 혈압 파형 임상데이터의 한계는 혈압파형과 심혈관계 건강상태 사이의 상관관계를 도출하고, 역추정에 활용하는데 어려움이 되는 원인이다(3).
이러한 혈압 파형 임상데이터의 부족을 극복하기 위하여 전산유체역학, 수치해석, 동물실험 등의 기법이 제시된다(5~7). 그러나 탄성의 관로 내에서 맥동하는 압력파의 연산은 많은 가정과 경계조건을 필수적으로 하여, 실제 인간의 그것을 재현하기 어렵고 임의의 추정치를 기반으로 한다.
이를 극복하기 위한 하드웨어 시뮬레이터 기반 혈압 파형 재현 연구가 진행되었다(8~10). 그러나 이들 대부분은 의료인 훈련을 위한 구조 모사체이거나, 혈압파형을 재현하더라도 형성원리가 아닌 펌프 구동 조절에 의존하는 한계가 있다(11).
이 연구에서는 인체 심혈관계의 구조와 물성을 모사하여, 혈압 파형의 형성과 전파를 재현하는 심혈관계 하드웨어 시뮬레이터를 개발하였다. 이를 통해 Fig. 1과 같이 중심-상완-요골 동맥 혈압 파형을 재현하였다.
이 연구의 심혈관계 하드웨어 시뮬레이터와 재현된 상완 및 요골 동맥 혈압 파형은 수치해석 모델과의 교차검증, 생체신호 발생 원리 규명, 상용 의료기기, 헬스 센서, AI 알고리즘의 검증과 성능평가 등에 활용이 가능하다.
2. 혈압 파형 형성 원리
2.1 전진파와 반사파의 중첩
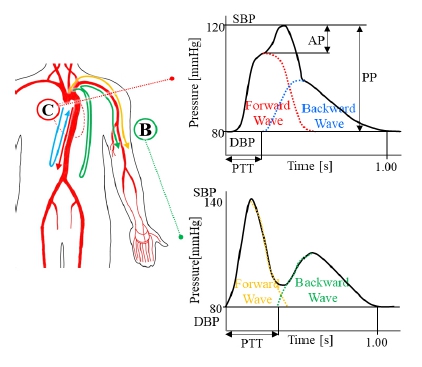
알려진 최고 120 mmHg, 최저 80 mmHg의 혈압은 대동맥궁에서 측정되는 중심동맥혈압에 기반한다. 중심동맥혈압 파형은 좌심실에서 생성된 전진파가 파복부의 대동맥 분기에서 반사되어 돌아오는 반사파와 중첩되어 형성된다고 알려져 있다(3).
이러한 전진파와 반사파의 중첩으로 인하여 상승하는 압력을 증강압(augmented pressure)이라고 하며, 2중 피크 형상의 파형과 120 mmHg의 최고혈압을 형성한다. 즉, 혈압 파형은 전진파와 반사파의 중첩으로 형성되며, 그 증거로 중심 대동맥 내에서 전파될 때 혈압 파형의 변화가 제시된다. Fig. 2의 상단은 중년의 경우, 중심 대동맥 내에서 전파되며 변화하는 혈압 파형을, 하단은 중심-상완-요골 동맥에서의 혈압 파형 변화를 나타낸다(3).
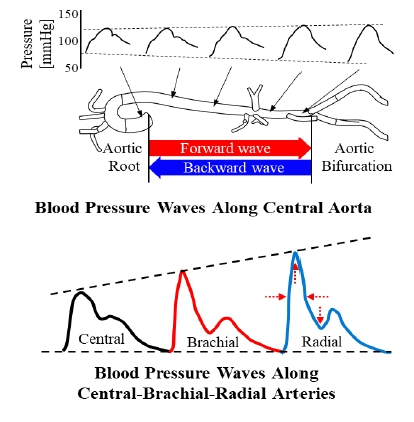
Blood pressure waveform changes according to propagation on the central aorta and brachial-radial arteries
혈압 파형에서 전진파와 반사파의 중첩 정도는 전파 거리와 전파 속도로 결정된다. 중심 대동맥에서 대동맥궁에서 반사파가 발생하는 대동맥 분기로 다가갈수록, 전진파와 반사파가 중첩되는 영역이 넓어지며 단일 피크의 형상으로 변화됨과 동시에 그 진폭이 커진다. 반면 중심-상완-요골 동맥 순으로 전파될 때, 보다 작은 직경의 상완, 요골 동맥을 통과하며 전진파의 진폭은 증가하고 그 폭은 좁아지는 수축기 증폭(systolic amplification)이 발생하며, 수축기 피크가 진폭이 증가하고 폭이 감소하는 것이 확인된다. 반면 전진파와 반사파 도달 사이의 경로 길이차는 일정하게 유지되므로 전진파와 반사파 간 시간차는 일정하게 유지되어, 중첩 영역이 감소하여 골이 깊어지는 현상이 나타난다.
2.2 맥파전파속도와 혈관 강성
혈관에서 혈압 파형의 전파 속도를 맥파전파속도(PWV, pulse wave velocity) 라고 한다. PWV는 전진파와 반사파의 전파속도를 결정하여, 둘의 중첩과 혈압 파형에 영향을 끼친다. 혈압파형을 탄성 관로 내 유체 압력 전파로 해석하였을 때, 파동 방정식과 그 전파속도를 유도할 수 있다(12). 혈압 파형이 형성, 전파되는 대동맥 및 동맥 구간은 직경 대비 두께가 10분의 1 이하인 얇은 벽과 20 cm/s 이하의 느린 유속으로 점성을 무시할 수 있는 조건이므로, 식 (1) ~ 식 (5)와 같이 유도가 가능하다.
| (1) |
| (2) |
| (3) |
| (4) |
| (5) |
식 (1)은 탄성 관로 내 질량 보존을, 식 (2)는 운동량 보존을 나타낸다. 각각을 시간과 길이방향으로 미분하여 대치할 경우, 식 (3)의 파동방정식을 유도할 수 있다. 이때 해당 파동의 전파속도는 압력과 단면적의 관계에 기반하며, 이는 식 (4)의 Hooke’s law로부터 유도할 수 있다. 이를 바탕으로 유도된 PWV는 식 (5)와 같다. E는 혈관 벽의 강성으로 노화에 따라 100 kPa ~ 1.5 MPa의 범위를 가지며, h는 혈관 벽의 두께, ρf는 혈액의 밀도, D는 혈관 내경, v는 혈관벽의 푸아송 비(Poisson’s ratio)이다. PWV는 혈관 벽의 강성과 두께에 비례하고, 혈관 벽의 직경과 혈액의 밀도에 반비례하며, 목의 경동맥과 허벅지의 대퇴동맥 사이에서 측정되는 cfPWV는 3 m/s ~ 15 m/s의 값을 가지며 노화에 따라 증가한다. 혈압 파형은 PWV에 의해 결정되며, 따라서 혈압 파형을 재현하기 위해서는 PWV를 인체와 똑같이 재현하기 위해 구조와 물성을 동일하게 재현해야 함을 뜻한다.
3. 심혈관계 시뮬레이터 개발
3.1 심혈관계 하드웨어 시뮬레이터 설계
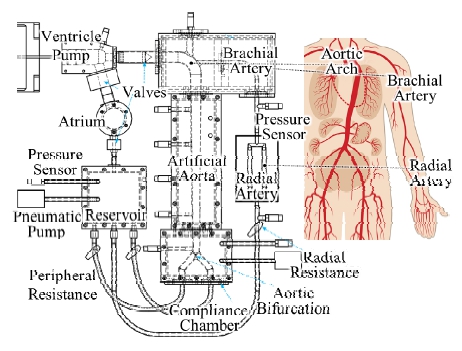
이 연구의 심혈관계 시뮬레이터는 인체 심혈관계의 생리학적 구조와 물성을 모사하여, 혈압 파형의 형성과 전파를 재현하는 것을 목표로 한다. 이를 위하여 인체와 동일한 심혈관계 건강상태로 구동될 수 있도록 설계되었다. 전진파를 형상하는 좌심실은 최대 120 bpm의 심박수와 최대 120 ml 박출량으로 구동이 가능한 리니어 펌프로 작동된다. 인체와 동일한 1대1 비율의 형상과 물성을 갖는 인공 대동맥 및 인공 상완, 요골동맥으로 연결된다. 인공 혈관부에서 재현된 동일한 PWV는 심실 펌프에서 발생한 전진파와 대동맥 분기에서 돌아오는 반사파가 전파, 중첩되며 혈압 파형을 형성하는 과정을 재현한다. 이후 정맥을 단순화한 정맥 탱크로 연결된다. 또한 각부 혈관의 말초저항을 조절할 수 있도록 볼밸브가 장착되며, 각부에 유압 센서가 장착되어 내부의 다양한 위치에서의 혈압 파형 신호를 획득한다.
이 연구의 시뮬레이터의 가장 큰 특장점중 하나는 가압 챔버 구조의 도입이다. 이는 생체 모사 실리콘으로 제작된 인공 혈관의 물성을 그대로 유지한 체, 혈압파형의 왜곡 없이 최고, 최저혈압을 자유롭게 조절을 가능케 하며, 이는 선행 논문에서 보다 자세히 설명되었다(13). 선행연구들의 인공혈관은 내압을 견디기 위하여 높은 강성을 갖는 노년의 혈압 파형만을 생성할 수 있지만, 이 연구의 가압 챔버를 통해 보다 약한 혈관 강성을 갖는 중년 및 청년의 혈압 파형 또한 재현 가능하다. 이 연구에서는 일반적으로 알려진 최고혈압 120 mmHg, 최저혈압 80 mmHg이며 이중 피크의 형상을 갖는 중년의 표준파형을 재현하는 것을 목표로 한다. 이를 위하여 60 bpm의 심박수와 70 ml의 박출량으로 구동되었으며, 중년의 PWV 6 m/s를 재현한다.
3.2 인공 대동맥, 상완 및 요골 동맥
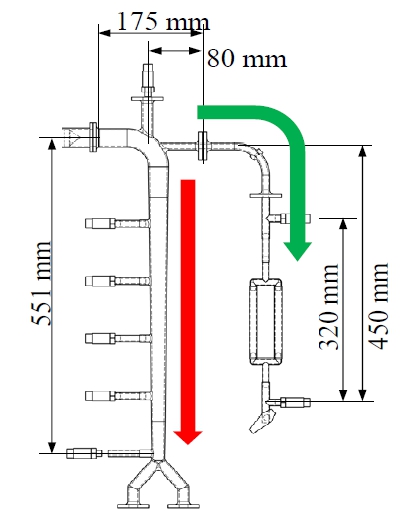
이 연구의 하드웨어 시뮬레이터는 Fig. 3과 같이 중심 대동맥을 모사한 인공 대동맥과, 상완 및 요골을 모사한 인공 동맥을 포함한다. 실제 인체 대동맥은 35 mm ~ 10 mm로 직경이 감소하며, 두께 또한 3 mm ~ 1 mm로 감소하고, 개개인마다 다른 복잡한 형상을 갖는다. 이 연구의 인공대동맥은 미 NHI에서 제시된 표준 수치를 기반으로 제작된 동맥계 3D 모델을 단순화하여 설계되었으며, 3D 프린터로 출력된 금형에 실리콘을 주입하여 injection molding을 통해 제작되었다.
대동맥궁의 내경은 28 mm, 대동맥 분기의 내경은 14 mm이며, 길이는 712 mm이다. 제작의 편의를 위하여 두께는 인간 대동맥 평균 두께와 동일한 2 mm로 통일되었다. 해당 치수로부터 중년의 PWV인 6 m/s를 재현하기 위해서는 PWV를 유도하는 식 (5)로부터 필요 실리콘의 강성을 계산할 수 있다. 유도된 목표 혈관 강성은 295 kPa이며, 해당 강성과 5 % 미만의 오차로 304 kPa의 강성을 갖는 SmoothOn(USA)의 SORTA-Clear 12 실리콘으로 제작되었다.
또한, 인공 상완 동맥은 인간과 동일한 내경 8 mm, 두께 1.5 mm로 제작되었다. 반면 인공 요골 동맥은 내경 10 mm, 두께 1 mm로 제작되었으며, 이는 인체 목표 치수인 직경 5 mm, 두께 0.5 mm의 각각의 2배에 해당한다. 이는 금형으로 제작 가능한 두께가 최소 1 mm인 점에서 비롯되며, 목표 치수와 동일한 PWV를 유지할 수 있도록 직경 또한 2배로 결정되었다.
4. 혈압 파형 재현
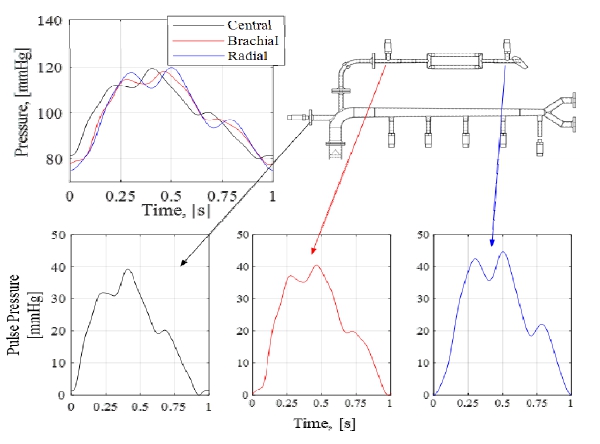
4.1 중심 동맥 혈압 파형 재현
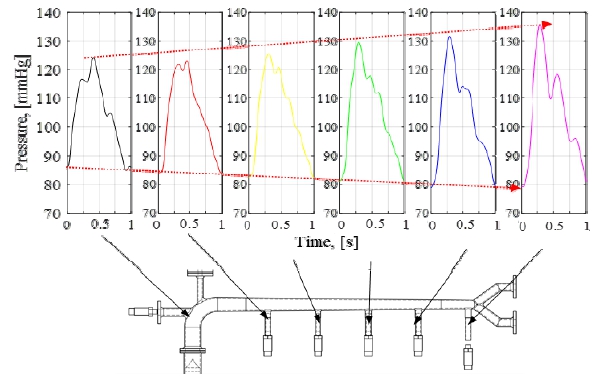
제작된 심혈관계 하드웨어 시뮬레이터와 인공 혈관을 바탕으로 중심, 상완, 요골 동맥 혈압 파형을 재현하였다. Fig. 4에서 적색 화살표를 따라 중심 대동맥 내부를 전파하며 변화하는 혈압 파형을 Fig. 5에 나타낸 것이다. 가장 좌측의 대동맥궁 내부 중심 혈압 파형은 중년의 혈압파형과 동일한 120 mmHg의 최고혈압과 80 mmHg의 최저혈압, 2중 피크 형상의 파형을 나타낸다. 이후 대동맥궁에서 대동맥 분기로 전파될수록, 전진파와 반사파의 중첩 영역이 넓어지며 최고혈압의 증가하고 단일 피크로의 파형변화 경향 또한 Fig. 2 상단과 동일하게 재현되었다. 인체와 동일한 물성과 구조의 재현을 통해, PWV 및 중첩으로 인한 혈압 파형의 형성을 재현했음을 나타내는 결과이다.
4.2 중심-상완-요골 동맥 혈압 파형 재현
또한 하드웨어 시뮬레이터의 인공 상완동맥 및 요골동맥에서 측정된 혈압파형을 인체와 비교하였다. Fig. 6은 Fig. 4에서 녹색 화살표를 따라 중심-상완-요골 동맥 내부를 전파하며 변화하는 혈압 파형을 나타낸 것이다. 인체에서, 중심동맥에서 상완, 요골동맥으로 전파될 수록, 감소하는 혈관의 직경으로 인하여 수축기 증폭 현상이 발생한다. 이는 전진파의 진폭을 증가시키며, 전진파의 시간 길이는 단축시킨다. 이는 수축기 최고혈압의 증가와, 반사파와 중첩되는 영역의 감소로 골이 깊어지는 형태의 파형 변화를 나타낸다. 이는 Fig. 2 하단과 동일한, 인체의 수축기 최고 혈압 상승, 중첩 영역 증강압 감소 등의 효과가 관측되었다. 이는 중심 동맥 혈압 파형과 마찬가지로 대동맥 분기에서 돌아오는 반사파가 상완 민 요골 동맥 파형을 결정함을 나타내는 증거이다. 이는 각부 수축기 피크-반사파 피크 사이 시간 지연이 일정하게 유지되는 것으로부터 확인할 수 있다.
5. 결 론
이 연구는 인체 심혈관계의 구조와 물성을 모사한 심혈관계 하드웨어 시뮬레이터를 이용하여, 중심 대동맥과 상완 및 요골동맥에서의 혈압 파형을 재현하였다. 재현된 혈압 파형은 인체와 동일한 크기와 파형, 변화 경향을 보였다. 이는 인공 혈관의 712 mm의 길이, 28 mm의 내경 및 304 kPa의 강성을 재현하는 것으로, 목표로 한 중년의 PWV인 6 m/s를 구현하여 전진파와 반사파의 중첩으로 인한 혈압 파형의 형성을 재현하는 것으로 달성한 결과이다. 단, 이 연구는 건강한 상태의 중년 단일 연령 및 강성에 대한 파형만을 재현하였으며, 다양한 임상 데이터와의 교차 검증이 필요하다. 후속 연구에서 청년의 낮은 혈관 강성과 노년의 높은 혈관 강성을 갖는 인공 대동맥과 동맥의 교체를 통해, 다양한 연령대의 혈압 파형을 재현 및 임상 데이터와 비교할 수 있다. 심박수, 박출량, 말초저항 등 시뮬레이터에서 조절 가능한 파라미터의 변경을 통해 다양한 심혈관계 건강 상태에 대한 혈압 파형을 생성할 수 있다.
이 연구의 이러한 성과는 향후 심혈관계 연구의 핵심 기술로서 다양한 연구로 확장될 수 있다(14). 상완부 및 손목 모의기(phantom)의 추가를 통해 혈압 파형 뿐만 아니라 PPG, 코르트코프 음, 혈압계 신호 등 다른 생체신호 데이터 생성으로 확장이 가능하다. 이는 부족한 임상 데이터를 보완하고, 관련 AI 연구에 활용되는 데이터베이스로 활용될 것이다. 또한 침습적, 비침습적 의료기기 및 헬스센서 임상 대체 테스트베드로 활용되며, 수술, 채혈 등 의료 술기 훈련 플랫폼으로 응용될 것이다. 또한, 인공 대동맥의 개선으로 건강한 상태뿐만 아니라 국부적으로 혈관 강성이 변화하는 대동맥류와 죽상경화를 포함하는 심혈관 질환의 원인과 증상에 대한 연구 또한 가능하다.
기 호 설 명
| A : | 단면적 |
| D : | 혈관 직경 |
| E : | 혈관 강성 |
| h : | 혈관 벽 두께 |
| P : | 압력 |
| Q : | 혈류량 |
| v : | 혈관 푸아송비 |
| ρf : | 혈액 밀도 |
| σ : | 응력 |
References
-
Schmitz, T. L. and Duncan, G. S., 2005, Three-component Receptance Coupling Substructure Analysis for Tool Point Dynamics Prediction, Journal of Manufacturing Science and Engineering, Vol. 127, No. 4, pp. 781~790.
[https://doi.org/10.1115/1.2039102]
- Ito, Y., 2008, Modular Design for Machine Tools, McGraw-hill Education.
-
Cao, H., Li, Y. and Chen, X., 2016, A New Dynamic Model of Ball-bearing Rotor Systems based on Rigid Body Element, Journal of Manufacturing Science and Engineering, Vol. 138, No. 7, 071007.
[https://doi.org/10.1115/1.4032582]
-
Brecher, C., Fey, M., Tenbrock, C. and Daniels, M., 2016, Multipoint Constraints for Modeling of Machine Tool Dynamics, Journal of Manufacturing Science and Engineering, Vol. 138, No. 5, 051006.
[https://doi.org/10.1115/1.4031771]
-
Heirman, G. H. K. and Desmet, W., 2010, Interface Reduction of Flexible Bodies for Efficient Modeling of Body Flexibility in Multibody Dynamics, Multibody System Dynamics, Vol. 24, pp. 219~234.
[https://doi.org/10.1007/s11044-010-9198-7]
-
Ahn, J.-G., Yang, H.-I. and Kim, J.-G., 2020, Multipoint Constraints with Lagrange Multiplier for System Dynamics and its Reduced-order Modeling, AIAA Journal, Vol. 58, No. 1, pp. 385~401.
[https://doi.org/10.2514/1.J058118]
-
Mokotoff, P. and Dannenhoffer, J., 2022, Exploring Tie Constraints for Structural Analysis Problems, Proceedings of AIAA SCITECH Forum.
[https://doi.org/10.2514/6.2022-0387]
-
Tsai, J.-S. and Chou, Y.-F., 1988, The Identification of Dynamic Characteristics of a Single Bolt Joint, Journal of Sound and Vibration, Vol. 125, No. 3, pp. 487~502.
[https://doi.org/10.1016/0022-460X(88)90256-8]
-
De Klerk, D., Rixen, D. J. and Voormeeren, S. N., 2008, General Framework for Dynamic Substructuring: History, Review and Classification of Techniques, AIAA Journal, Vol. 46, No. 5, pp. 1169-1181.
[https://doi.org/10.2514/1.33274]
- Cuppens, K., Sas, P. and Hermans, L., 2001, Evaluation of the FRF based Substructuring and Modal Synthesis Technique Applied to Vehicle FE Data, Proceedings of the International Seminar on Modal Analysis, Vol. 3, pp. 1143~1150.
- Allemang, R. J., 2003, The Modal Assurance Criterion – Twenty Years of Use and Abuse, Sound and Vibration, Vol. 37, No. 8, pp. 14~21.
- Van der Seijs, M. V., Van den Bosch, D. D., Rixen, D. J. and de Klerk, D., 2013, An Improved Methodology for the Virtual Point Transformation of Measured Frequency Response Functions in Dynamic Substructuring, Proceedings of 4th ECCOMAS Thematic Conference on Computational Methods in Structural Dynamics and Earthquake Engineering, Vol. 4, pp. 4334~4347.
-
Solmaz, S., Kester, L. and Van Gerven, T., 2023, An Immersive Virtual Reality Learning Environment with CFD Simulation: Unveiling the Virtual Garage Concept, Education and Information Technologies, Vol. 29, pp. 1455~1488.
[https://doi.org/10.1007/s10639-023-11747-z]
-
Albertelli, P., Goletti, M. and Monno, M., 2013, A New Receptance Coupling Substructure Analysis Methodology to Improve Chatter Free Cutting Conditions Prediction, International Journal of Machine Tools and Manufacture, Vol. 72, pp.16~24.
[https://doi.org/10.1016/j.ijmachtools.2013.05.003]
-
Kang, S., Yang, S., Kim, S. J., Ju, H. J. and Kang, Y. J., 2020, Engine Mount Response Improvement using Hybrid Modeling and Bayesian Optimization, Transactions of the Korean Society for Noise and Vibration Engineering, Vol. 30, No. 6, pp. 546~552.
[https://doi.org/10.5050/KSNVE.2020.30.6.546]
-
Klaassen, S. W. B., Van der Seijs, M. V. and De Klerk, D., 2018, System Equivalent Model Mixing, Mechanical Systems and Signal Processing, Vol. 105, pp. 90~112.
[https://doi.org/10.1016/j.ymssp.2017.12.003]
-
Kim, J. G., Nam, K.-U. and Kang, Y. J., 2020, Method to Estimate Rotational Stiffness: Trial Masses, Virtual Masses, and Virtual Springs, Journal of Sound and Vibration, Vol. 477, 115321.
[https://doi.org/10.1016/j.jsv.2020.115321]
-
Özşahin, O., Budak, E. and Özgüven, H. N., 2015, Identification of Bearing Dynamics under Operational Conditions for Chatter Stability Prediction in High Speed Machining Operations, Precision Engineering, Vol. 42, pp. 53~65.
[https://doi.org/10.1016/j.precisioneng.2015.03.010]
-
Kono, D., Nishio, S., Yamaji, I. and Matsubara, A., 2015, A Method for Stiffness Tuning of Machine Tool Supports Considering Contact Stiffness, International Journal of Machine Tools and Manufacture, Vol. 90, pp. 50~59.
[https://doi.org/10.1016/j.ijmachtools.2015.01.001]

Jae-Hak Jeong received B.S. degree in mechanical engineering from Yonsei University in 2017, M.S. degree in mechanical engineering from Korea Advanced Institute of Science and Technology (KAIST) in 2019, and Ph.D. degree in mechanical engineering from Korea Advanced Institute of Science and Technology (KAIST) in 2024. His research interests include cardiovascular system, biomimetics, bio-signal processing and hemodynamics.

Yong-Hwa Park joined KAIST in 2016 as an Associate Professor of the department of mechanical engineering devoting to research on vibration, acoustics, vision sensors, and recognitions for human-machine interactions. His research interests include structural vibration; event/condition recognition from sound and vibration signatures utilizing AI; blood pressure and health monitoring sensors; 3D sensors and lidar for motion measurements.